식품의약품안전처(처장 이의경) 식품의약품안전평가원은 2018년 ‘바이오의약품 표준화 분야 WHO(세계 보건기구) 협력센터’ 연차보고서를 발간·배포 한다고 17일 밝혔다.
해당 연차 보고서에는 지난해 수행한 ▲WHO 가이드라인 및 권고사항 제‧개정 지원 ▲국제표준품 및 시험법 관련 국제 공동연구 ▲개발도상국 규제기관 역량강화를 위한 교육훈련 ▲서태평양지역 등에서 WHO 가이드라인 이행 촉진 등과 관련된 주요 성과가 담겼다.
보고서에 따르면 ’바이오시밀러 질의응답 관련 가이드라인‘ 등 바이오의약품 분야 WHO 가이드라인 47건에 대한 기술자문과 ’빈혈치료제 표준품’ 등 56건의 WHO 국제표준품(바이오의약품을 시험할 때 기준으로 사용하는 물질) 개발 공동연구를 수행했다.
또 개발도상국의 바이오의약품 분야 규제역량강화를 위해 WHO에서 국제교육훈련센터로 지정받아 GMP 심사관 교육, 국가출하승인 교육, 백신 장비 교육 등 총 37개국 230명을 교육했다.
이 외에도 ‘WHO 바이오의약품 GMP 이행워크숍’ 등 국제기준의 이행을 위해 WHO와 공동으로 총 9건의 국제회의를 개최했다.
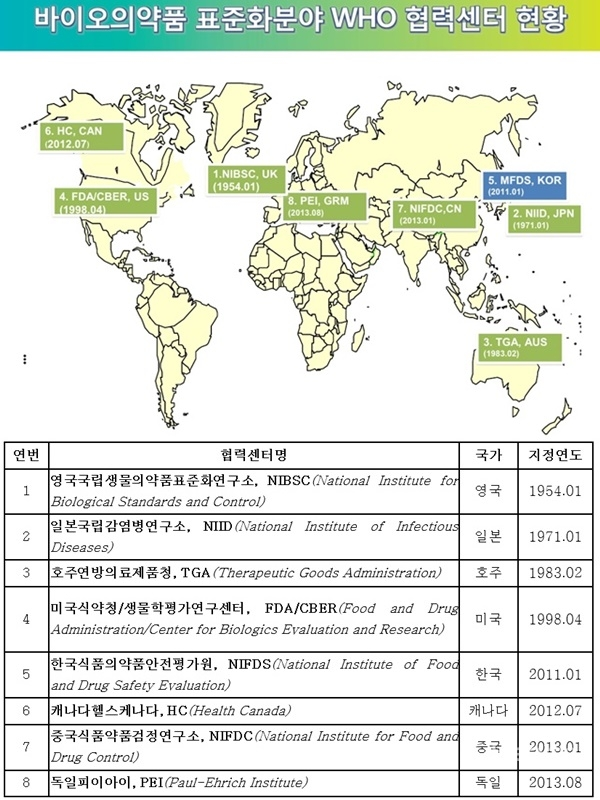
앞서 식품의약품안전평가원은 지난 2011년 영국, 일본, 미국 등에 이어 세계 5번째 ‘바이오의약품 표준화 분야’ WHO 협력센터로 지정받았고, 2018년 제3회 서태평양지역 WHO 협력센터 포럼에서 우수 WHO 협력센터로 수상한 바 있다.
식품의약품안전평가원은 “이번 2018년 연차보고서를 국문 뿐 아니라 영문으로 발간할 예정이며, 바이오의약품 표준화 분야를 선도하는 기관으로 위상을 높이기 위해 지속적으로 노력하겠다”고 밝혔다.